Guide synthétique de l'approche européenne pour la prise en charge médicale et thérapeutique des irradiations de masse
Gestion thérapeutique – en accord avec la conférence européenne de consensus nommée « European approch for medical management of mass radiation exposure » - actualisé en octobre 2017
En 2007, un consensus européen a été établi sur une méthode de prise en charge médicale en cas d’accident d’irradiation de masse. Il était l’aboutissement d’une démarche commune de l’EBMT (European Society for Blood and Marrow Transplantation), de l’IRSN et de l’Université d’Ulm (Allemagne) qui, réunissant les référents européens principalement en hématologie, a permis d’élaborer des contre-mesures médicales notamment dans le cas des aplasies radio-induites.
L’IRSN est membre du NAC (Nuclear Accident Commitee) de l’EBMT, et y contribue notamment via ses recherches sur le traitement des aplasies radio-induites et par ses capacités de conseil dans la gestion des accidents d’irradiation.
Que peut offrir l'EBMT-NAC pour la gestion des accidents d'irradiation de masse ?
Un réseau compétent de 500 centres et départements d’hématologie pour des conseils sur :
- Le tri des irradiés et leur prise en charge médicale
- L’évolution clinique des symptômes L’optimisation des soins en-dehors des frontières nationales
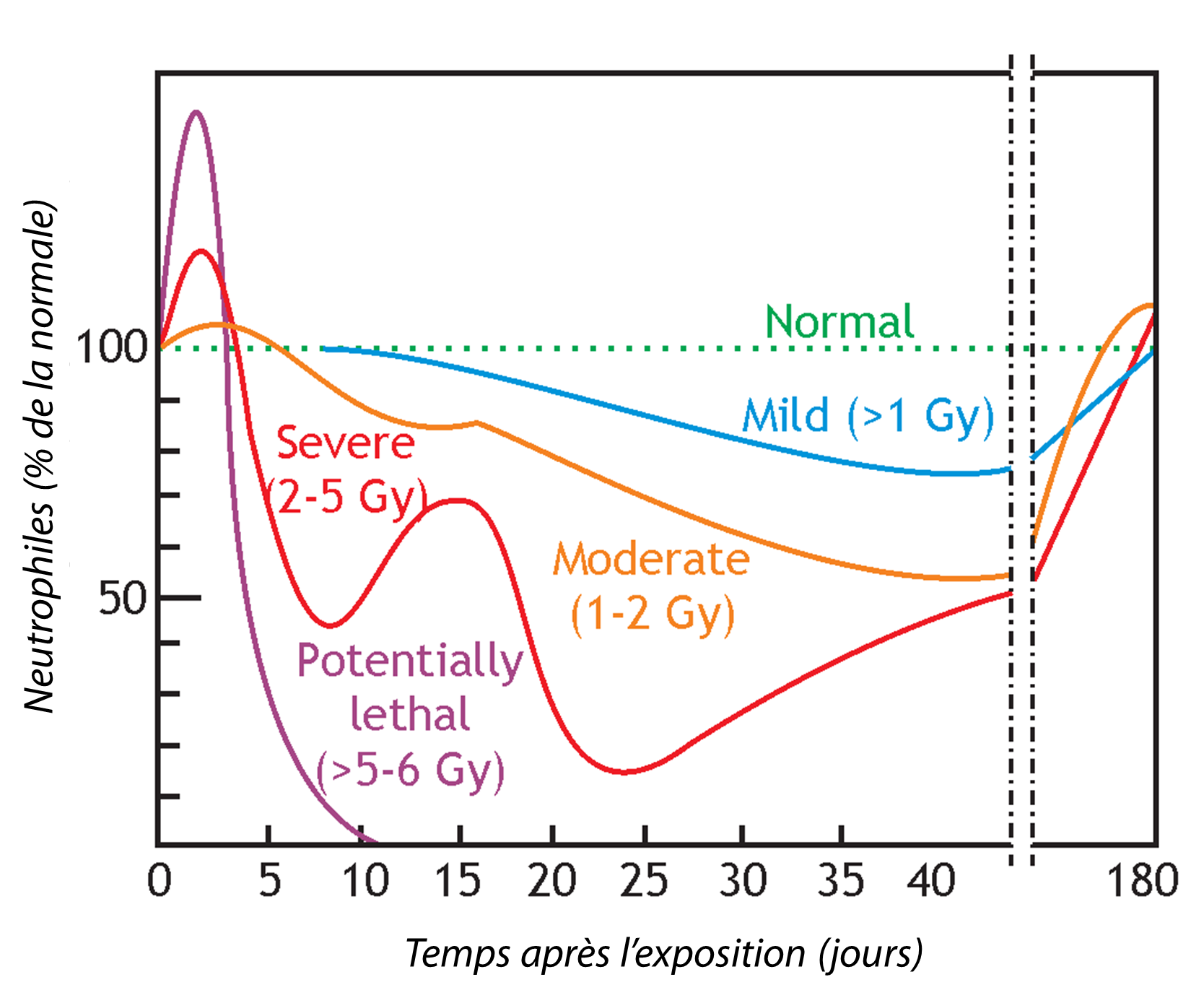
La quantité d'énergie absorbée par les organes du corps est mesurée en Gray (Gy) ; l'effet de cette irradiation est donnée par la dose équivalente mesurée en Sievert (Sv). Pour les rayons X et les particules bêta 1 Gray ≈ 1 Sievert.
Déroulement du protocole de prise en charge d’un accident d’irradiation de masse
Les premières 48 heures suivant l’accident
Rappel
- Il faut décontaminer après la stabilisation clinique du patient.
- Le traitement des urgences chirurgicales ou médicales (brûlures) est prioritaire en toutes circonstances et l’évaluation de la dose d’irradiation doit se faire dans un second temps.
- L’irradiation n’est pas une contamination – Un irradié n’est pas source d’irradiation.
Blessures graves dues aux irradiations
La sévérité des signes cliniques prodromiques est un indicateur de la gravité des lésions :
- Erythème étendu et immédiat
- Syndrome précoce d’incapacité passagère (perte de conscience temporaire)
- Forte fièvre
- Hypotension, vomissements précoces
- Diarrhée immédiate
Caractérisation de l'accident
- Enquête : circonstances de l’accident (irradiation avec ou sans contamination, utilisation d’un appareil de contrôle de la contamination), caractéristiques de la source d’irradiation, distance source-victime, durée d’exposition, si l’irradiation est homogène ou hétérogène.
- Etiquetage et stockage des vêtements et affaires personnelles ainsi que des matériaux biologiques (cheveux, ongles).
Prélèvements d'urgence
- Hémogramme (avec des différentiels) toutes les 4 à 8 heures dans les premières 24 heures puis toutes les 12-24 heures les jours suivants.
- Typage du groupe sanguin.
- Tests biochimiques standards et vérification du taux d’amylasémie.
- Prélèvements d’urines et selles si une contamination aux radionucléides est suspectée.
- Stockage de sérum et cellules ou ADN pour des analyses plus approfondies incluant un typage HLA.
- Recherche d’aberrations chromosomiques sur les lymphocytes sanguins (dosimétrie biologique) (15ml + héparine). Demander conseil auprès des réseaux nationaux ou internationaux de dosimétrie biologique.
Première classification sur les signes cliniques
Noter sur une feuille horodatée l'apparition des symptômes
| | Grade I | Grade II | Grade II |
|---|---|---|---|
| Délais moyen avant l'apparition des symptômes | Inférieur à 12 heures | Inférieur à 5 heures | Inférieur à 30 minutes |
| Erythème cutané | 0 | +/- | +++ ; avant la 3ème heure |
| Asthénie/Faiblesse | + | ++ | +++ |
| Nausées | + | +++ | (-) |
| Vomissements par 24h | Maximum 1 | 1 à 10 | Plus de 10 / Incoercibles |
| Diarhée / Nombre de selles par 24h | 2 à 3 maximum ; dures | 2 à 9 ; molles | Plus de 10 ; liquides |
| Douleurs abdominales | Minimales | Intenses | Insoutenables |
| Céphalées | 0 | ++ | Insoutenables ; signes d'H.T. intracrânienne |
| Température | Inférieure à 38°C | 38-40°C | Supérieure à 40°C |
| Pression sanguine | Normale | Normale - possible baisse temporaire | Systolique inférieure à 80 |
| Pertes de consciences temporaires | 0 | 0 | + / coma |
| Chute des lymphocytes circulants | |||
| Numération à 24h | Supérieur à 1500/µl | Inférieur à 1500/µL | Inférieur à 500/µl |
| Numération à 48h | Supérieur à 1500/µl | Inférieur à 1500/µl | Inférieur à 100/µl |
| | Surveillance ambulatoire | Hospitalisation pour un traitement curatif | Hospitalisation Syndrome de défaillance multi-organe |
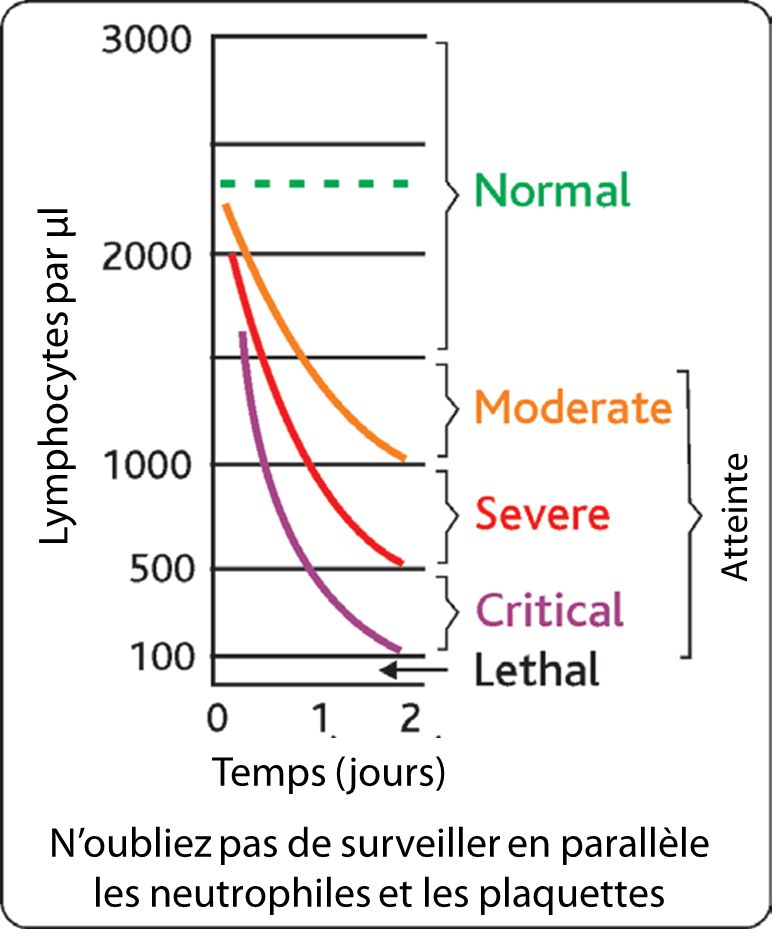
Au-delà de 48 heures après l'accident
Au-delà des premières 48h, un second score clinique est effectué sur les organes (hématopoïétiques, gastro-intestinaux, cutanés, neuro-vasculaires) selon le protocole international METROPOL (Medical Treatment Protocols for radiation accident victims) pour la gestion thérapeutique et la prédiction du syndrome de défaillance multiviscérale.
Traitement aux cytokines
Grade I : Surveillance, pas de traitement aux cytokines
- Surveillance clinique en ambulatoire.
- Numération sanguine les 2 premiers jours puis une fois par semaine durant 2 mois.
Grade II : Traitement aux cytokines (curatif)
- Du G-CSF doit être administré sous 48h ou dès que possible jusqu’au rétablissement du nombre de neutrophiles (ANC>0.5x109/l). Des agonistes d’EPO (érythropoïétine) et de TPO (thyroperoxydase) peuvent être utilisés si nécessaire. Soutien habituel à la défaillance de la moelle osseuse par des antibiotiques, des produits sanguins et par les traitements hémato-oncologiques usuels.
- Traitement symptomatique de l’atteinte gastro-intestinale.
- Si aplasie sévère -> environnement protégé.
- L’exposition accidentelle aux radiations est généralement hétérogène. Certaines régions sous-exposées ou protégées de la moelle osseuse peuvent entrainer un rétablissement hématopoïétique endogène.
Grade III : Cytokines (jusqu’à réévaluation du grade)
- Les patients sont traités comme pour le grade II jusqu’à confirmation du grade III.
- Soins palliatifs et de fin de vie à initier.
- Réévaluation durant la première semaine sur des tests en laboratoire ou sur des signes cliniques révélateurs de dommages irréversibles ou de défaillance multiviscérale.
N.B. Les brûlures radiologiques graves ont une évolution torpide particulière. Leur traitement nécessite une consultation spécialisée.
Greffe de cellules souches hématopoïétiques (CSH)
Préambule
- La greffe CSH n’est pas une urgence.
- Il est crucial d’éviter un GVHD (Graft versus Host Desease) pour ne pas compromettre un rétablissement endogène.
- Si une sévère aplasie persiste sous traitement aux cytokines durant plus de 14 jours, la possibilité d’une greffe de cellules souches hématopoïétiques doit être discutée (voir ci-dessous).
Critères d’inclusion
- Sévère aplasie médullaire persistant durant 14 à 21 jours malgré le traitement aux cytokines.
- Pas d’hématopoïèse résiduelle dans la biopsie ostéo-médullaire.
- Absence de signe clinique d’autre organe endommagé de manière irréversible.
- Si une infection est présente, elle est traitée et contrôlée.
Le Greffon
- Type de greffon :
- - Moelle osseuse
- CHS du sang périphérique (déplété ou non)
- Sang placentaire
- - Moelle osseuse
- Donneur par ordre de préférence (conformément aux critères de greffe actuels) :
- Frère ou sœur HLA identique au patient
- Donneur non-apparenté HLA identique au patient
- Sang placentaire avec une correspondance supérieure à 4/6
- Haplo-identique au patient - Doses de cellules à greffer :
- Au moins 2x106 cellules CD34 par kg (cytaphérèse)
- Au moins 2x108 cellules nucléées par kg (moelle osseuse)
- Au moins 3x107 cellules nucléées par kg (sang ombilical)
Conditionnement et prévention du GVH (conformément aux critères de transplantation actuels) :
- Conditionnement non myélo-ablatif
- Pas de méthotrexate
Références :
- Gorin NC et al - Consensus conference on European preparedness for haematological and other medical management of mass radiation accidents, Annals of Hematology 85 : p671-679, 2006.
- Fliedner TM et al – Medical Management of Radiation Accidents - Manual of the acute radiation syndrome, published by BIR, 2001.
- Powles R et al – The role of the European haematologist in a large irradiation emergency: the European Blood and Marrow Transplantation Society (EBMT) Nuclear Accident Committee (NAC), Health Phys, 98 : p810-814, 2010.
Avant ce consensus, la gestion des accidents d’irradiation était conçue pour les sites où les risques étaient identifiables et impliqueraient un nombre limité de victimes. Cependant, en cas d’accident majeur ou d’acte de malveillance, un grand nombre de victimes irradiées pourraient nécessiter une prise en charge médicale. Sans préparation à cette situation exceptionnelle, les équipes médicales auraient une très forte pression pour définir le diagnostic et le traitement approprié.
Le consensus européen définit une méthode pour diagnostiquer et prendre en charge les victimes selon leur état. Elle se base en particulier sur un « tri » des victimes irradiées grâce à l’évaluation des signes cliniques afin d’adapter la prise en charge thérapeutique.
