Le projet INTRUST
Le projet INTRUST (INnovations Therapeutiques Pour Le Traitement Du Syndrome Gastrointestinal Radio-Induit) vise à mettre en place des contre-mesures médicales innovantes pour la prise en charge d’une exposition radiologique induisant une défaillance intestinale aiguë.
Le projet lancé en 2020 pour une durée de 3 ans est piloté par l’IRSN et implique également le Laboratory for Vascular Translational Science et le Centre de Recherche sur l’Inflammation, deux laboratoires de l’INSERM.
Le projet INTRUST a été sélectionné dans le cadre du programme ASTRID (Accompagnement Spécifique des travaux de Recherches et d’Innovation Défense) de l’Agence Nationale de la Recherche (ANR) et de l’Agence de l’innovation de défense (AID) qui vise à soutenir les projets à caractère fortement exploratoire et innovant dont les retombées peuvent être à la fois civiles et militaires.
Caractéristiques du projet
Dates de réalisation : 2020-2023
Financement : 300 000 euros
Partenaires : IRSN - Laboratory for Vascular Translational Science (INSERM) - Centre de Recherche sur l’Inflammation (INSERM)
Contexte
Le syndrome gastro-intestinal (SGI) apparait lors d'une exposition du corps sur un grand volume à des rayonnements ionisant de plus de 6 Gy. Elle provoque une rupture de la barrière épithéliale de l'intestin, ce qui favorise la pénétration d'agents pathogènes et active une forte réaction inflammatoire. La prise en charge de ce SGI reste confrontée à un mur thérapeutique.
Les études précliniques sur la mise en place de mesures médicales sont toutes basées sur des approches mono-thérapeutiques avec des résultats souvent décevants et aucun consensus scientifique sur une solution thérapeutique pour la prise en charge du SGI n'existe aujourd'hui.
Les lésions intestinales radio-induites du SGI sont très proches de celles observées chez des patients atteints de maladies inflammatoires chroniques de l'intestin (MICI), comme la maladie de Crohn ou la rectocolite hémorragique. En effet, elles partagent des symptômes identiques (douleurs abdominales, diarrhées fréquentes, saignements) associés à une inflammation du tube digestif et la destruction de l'épithélium intestinal. La vision clinique contemporaine des MICI s'oriente vers des approches multimodales qui pourraient être appliquées au SGI, en raison des caractéristiques physiopathologiques communes à ces deux maladies.
C'est pourquoi le projet INTRUST propose une approche basée sur l'hypothèse que seul un traitement global et multimodal pourrait être réellement efficace, robuste et accessible à un nombre important de victimes pour le traitement du SGI.
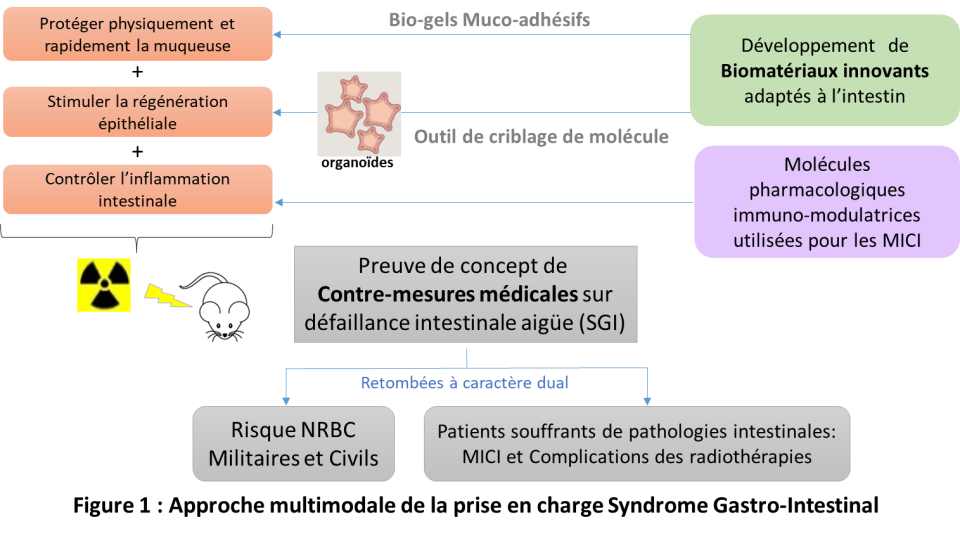
Le projet vise à démontrer l'intérêt et la faisabilité d'une approche thérapeutique ciblant 3 composantes essentielles à prendre en compte pour une stratégie thérapeutique efficace: agir rapidement après l'irradiation pour protéger physiquement la muqueuse intestinale, associer des agents thérapeutiques régénérant la muqueuse digestive et contrôler l'inflammation intestinale par des immuno-modulateurs.
Photo : approche mutlimodale de la prise en charge Syndrome Gastro-Intestinal - © Médiathèque IRSN
Axes de recherche
Le programme scientifique du projet est décomposé en 4 workpackages (WP) :
WP1 : Développement de biomatériaux innovants pour une application in vivo et in vitro
L'objectif du WP1 est de développer un bio-gel muco-adhésif (BGMA) compatibles avec la médecine réparatrice et un biomatériau utilisé pour la formation d'organoïdes intestinaux humains in vitro.
Afin d'éviter un choc septique, il est essentiel de maintenir la barrière physique qui protège l'organisme des bactéries intestinales. Cette barrière est normalement constituée par une couche de mucus riche en glycoprotéines qui forment un réseau de polymères. Le projet INTRUST a pour objectif de développer un BGMA mimant les propriétés de cette couche de mucus. Dans le cadre du SGI, le bio-gel doit être rapidement appliqué sur l'ensemble de l'intestin. C'est pourquoi le WP1 se charge également d'étudier les voies d'administration les plus efficaces. Les solutions envisagées sont l'application directe par endoscopie ou par voie orale avec la conception d'une gélule contenant les composants qui permettront de former le bio-gel dans l'intestin par un recouvrement progressif.
En parallèle, le WP1 doit préparer le biomatériau servant de matrice pour la culture des organoïdes. Cette matrice doit apporter aux cellules un environnement similaire à celui de la matrice extracellulaire de l'organe d'origine afin de permettre la prolifération et la différenciation des cellules. Toutefois, le Matrigel, un hydrogel provenant de matrice extracellulaire sécrétée par des cellules animales cancéreuses, traditionnellement utilisé dans la culture des organoïdes, peut perturber les expérimentations menées sur les organoïdes à cause de son caractère tumoral. Le biomatériau développé par le WP1 vise à pallier à ce déficit.
WP2 : Mise en place de l'outil "organoïdes" et criblage de molécules régénératrices
Cet axe de recherche est consacré à l'étude des effets de molécules de régénération épithéliale et de produit de thérapie cellulaire sur des organoïdes qui auront été préalablement irradiés afin de reproduire les conditions d'un SGI. Le projet vise à favoriser la plasticité des cellules de l'épithélium intestinal et à stimuler la différenciation des cellules souches présentes dans les cryptes intestinales qui sont impliqué dans le renouvellement naturel des cellules de l'intestin.
WP3 : Validation in vivo de l'effet protecteur des bio-gels muco-adhésifs (BGMA)
Les travaux réalisés dans le cadre du WP3 visent à valider l'efficacité du biomatériau sélectionné dans le cadre du WP1 pour la conception du bio-gels muco-adhésifs en se basant sur un modèle animal, la souris.
Cet axe de recherche doit également évaluer la possibilité de contrôler l'inflammation de l'intestin en incorporant des immuno-modulateurs dans le BGMA. Le couplage d'un anti-inflammatoire au bio-gel permettrait d'obtenir un effet optimisé sur la préservation de l'intégrité de la barrière au moyen de la protection physique du bio-gel, de l'effet anti-inflammatoire qui permettrait de "fermer" les jonctions serrées épithéliales et de la diminution la translocation bactérienne et l'inflammation résultante. Le couplage permettrait également de minimiser la diffusion d'anticorps dans les selles et de maximiser sa durée de vie et son action locale.
Enfin le WP3 évaluera l'efficacité et les propriétés adhésives du bio-gel en fonction des différentes méthodes d'administrations prévu par le WP1.
WP4 : Validation in vivo du traitement multi-modal sur modèle animaux SGI et MICI
Le dernier axe du projet INTRUST a la charge de valider l'efficacité de l'association des traitements mis en place dans les workpackage 1 à 3 sur des modèles pré-cliniques de lésions digestives radio-induites (SGI) ou inflammatoires chroniques (MICI).
Dans un premier temps il s'agira de valider, sur un modèle de lésions digestives radio-induites, l'efficacité thérapeutique des molécules régénératrices de la muqueuse identifiée dans le WP2 associé au BGMA issus du WP3. Dans un second temps le WP4 intégrera et les immuno-modulateurs et évaluera les bénéfices thérapeutiques de ce traitement multimodal.
La validation de ce traitement s'appuiera sur la perméabilité intestinale au moyen de molécule fluorescente, sur la capacité de régénération de la muqueuse par comptage des cryptes intestinales et sur la prolifération de cellules souches, identifiées par immunomarquage.
Les laboratoires impliqués
laboratoires : Laboratoire de radiobiologie des expositions médicales (LRMed)

LRMED
L'objectif du LRMed est d’acquérir de nouvelles connaissances sur les mécanismes biologiques d’initiation et de progression des lésions localisées sur les tissus sains résultant d’expositions aux rayonnements ionisants, à des doses modérées et fortes, utilisées dans le domaine médical à des fins diagnostiques ou thérapeutiques (e.g radiothérapie) pour mieux prédire les risques de complications, mieux les comprendre, les prévenir et les traiter.
En savoir plus
-
Contact
